xHyA
vernetzte hyaluronsäure
Hyaluronsäure (HA) ist eine physiologische Substanz und stellt eine der Hauptkomponenten der außerzellulären Matrix des Bindegewebes, der Gelenkflüssigkeit und vieler anderer Gewebe dar.1-3
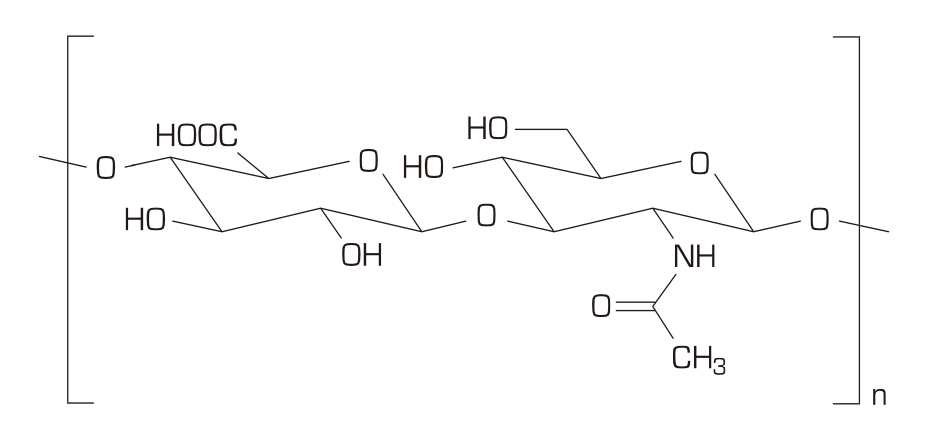
Biochemisch betrachtet ist HA ein natürliches Polysaccharid-Makromolekül (geradkettiges Glycosaminoglykan).
PHYSIOLOGISCHE FUNKTIONEN VON HYALURONSÄURE
HA besitzt wichtige hygroskopische, rheologische und viskoelastische Eigenschaften und übt damit zahlreiche physiologische und strukturelle Funktionen aus.
Außer der vordringlichsten Aufgabe als „Schmiermittel“ in Gelenken spielt HA eine wichtige Rolle bei den grund- legenden regenerativen Prozessen, wie der Wundheilung und Embryogenese.
HA ist insbesondere bei solchen Situationen entscheidend, in denen eine schnelle Geweberegeneration und -reparatur erfolgen.4
Die einzelnen Funktionen der HA unterscheiden sich grundlegend in Abhängigkeit von der jeweiligen molekularen Größe (Kettenlänge).
Lange Hyaluronsäure-Ketten sind im Allgemeinen durch ihre immunsuppressiven, antiangiogenen und entzündungshemmenden Eigenschaften an der Modulation der Immunreaktion beteiligt. Kürzere Hyaluronsäure-Ketten sind dahingegen relevant für die Wund- und Gewebeheilung, da sie angiogene, immunstimulierende und inflammatorische Eigenschaften aufweisen.4,5
ANWENDUNGSGEBIETE
Umfangreiche Studien haben gezeigt, dass HA ein ideales Biomaterial für kosmetische, medizinische und pharmazeutische Anwendungen darstellt.
Neben ihrer ausgeprägten regenerativen Wirkung bindet HA Flüssigkeiten (1g Hyaluronsäure kann bis zu 6l Wasser aufnehmen).6 Durch die stark viskose Konsistenz unterstützen HA-Gele bei chirurgischer Anwendung die Wundraumstabilisierung. Je nach Indikation und angestrebter Funktion wird HA entweder in natürlicher Form oder mit zusätzlicher Kreuzvernetzung verwendet. Natürliche Hyaluronsäure weist das höchste regenerative Potenzial auf. Sie wird innerhalb von wenigen Stunden bis zu einigen Tagen in vivo abgebaut. Durch Vernetzung von natürlicher HA kann das Abbauverhalten bis zu mehreren Monaten verlängert werden. Allerdings wird vernetzte HA durch Reduzierung ihrer physiologischen Eigenschaften mehr und mehr inert.
KONZEPT
Optimiert für den regenerativen Behandlungserfolg
Vernetzte Hyaluronsäure in pharmakologischer Qualität (xHyA) zeichnet sich durch ein langsames Resorptionsprofil aus (mehrere Wochen) und grenzt sich somit von konventionellen Hyaluronsäure-Präparaten ab.
Diese weisen entweder einen deutlich höheren Vernetzungsgrad und somit ein längeres Abbauprofil auf (z.B. dermale „Filler“ in der Ästhetischen Chirurgie) oder sind nicht vernetzt und werden sehr schnell resorbiert (z.B. nicht-chirurgische HA-Präparate für die topische Anwendung).
Durch die Kombination von HA-Kettenlänge und speziell eingestellten Vernetzungsgrad wird bei xHyA das große regenerative Potenzial natürlicher Hyaluronsäure erhalten. Zugleich wird gewährleistet, dass xHyA nach Applikation nicht zu schnell abgebaut wird, und so während der verschiedenen Phasen des Heilungsprozesses präsent ist.7 Studien haben gezeigt, dass die verlängerte Anwesenheit von Hyaluronsäure während des Heilungsprozesses die Heilung durch Regeneration und nicht durch Reparation fördert.8-11

Vorteile
- Beschleunigte kontrollierte Wundheilung
- Stabilisierung und Schutz des Wundraums
- Unterstützung der Geweberegeneration
TECHNOLOGIE
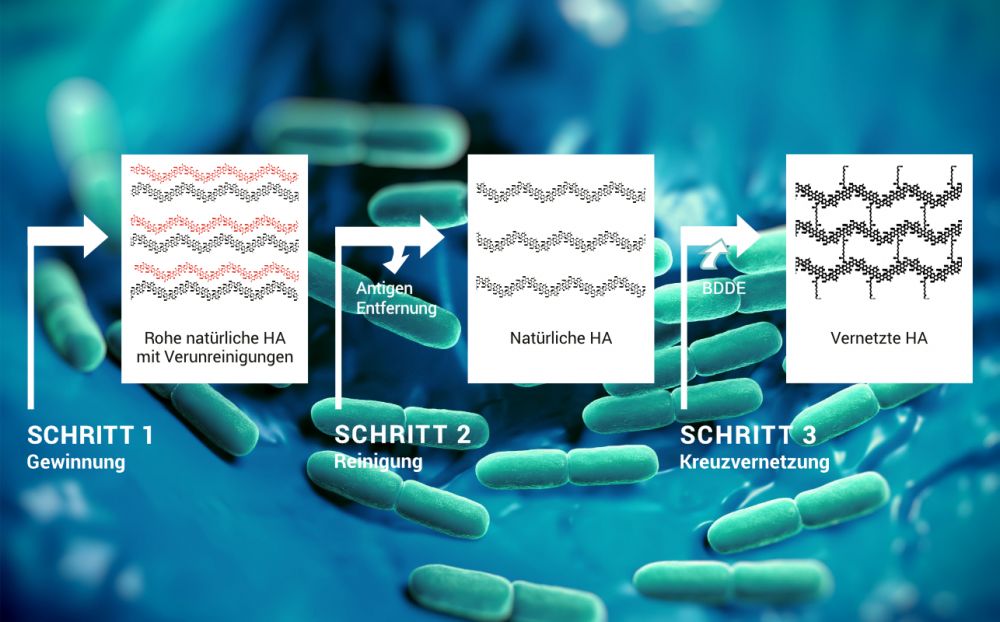
Schritt 1: Gewinnung
Reine Hyaluronsäure ist bei allen Spezies gleich,4 was die Gewinnung für die exogene Anwendung erleichtert. Traditionell wird HA aus Hahnenkämmen und der Augenflüssigkeit von Rindern extrahiert. HA bildet allerdings einen Komplex mit anderen Makromolekülen, sodass die Isolation einer bestimmten HA-Qualität aus diesen Quellen schwierig zu bewerkstelligen ist. Infolgedessen weist die HA tierischer Herkunft eine variierende Zusammensetzung auf.12 Zudem wird der Verwendung von tierischen Substanzen für die Behandlung beim Menschen wachsender Widerstand aufgrund ethischer Argumente und möglichem Risiko einer Virus-Infektion entgegengebracht.
Moderne Technologien, HA zu gewinnen, basieren auf der Anwendung eines bakteriellen Fermentationsprozesses ohne die Verwendung tierischer Gewebe.13
Bei der biotechnologisch hergestellten HA können die polymeren Eigenschaften sehr genau kontrolliert werden. Dies ermöglicht eine homogene HA-Zusammensetzung auf sichere und umweltfreundliche Art.
Schritt 2: Reinigung
Die sorgfältige Aufreinigung der so gewonnenen Hyaluronsäure spielt eine entscheidende Rolle dabei, zurückgebliebene bakterielle Proteine zu entfernen. Letztere können antigene Eigenschaften aufweisen und so eine Empfängerreaktion hervorrufen.14
Schritt 3: Kreuzvernetzung
Während natürliche HA-Komponenten im Allgemeinen einem schnellen Abbau unterliegen, benötigen viele erfolgreiche Therapieverfahren eine längere Verweildauer im Körper. Um das Resorptionsprofil der HA-Derivate zu verlängern, wird natürliche HA mittels bewährter chemischer Technologien vernetzt. Der Grad der Vernetzung beeinflusst sowohl die Abbauzeit als auch die physiologische Wirksamkeit. Die etablierteste Methode ist die Anwendung von BDDE (Butandioldiglycidylether) als Vernetzungs-Agens. Die Kehrseite der Verwendung von BDDE besteht darin, dass Rückstände im HA-Implantat Nebenwirkungen hervorrufen können. Daher ist die sorgfältige Reinigung von vernetzter HA elementar.15
LITERATUR
- Lee JY, Spicer AP. Curr Opin Cell Biol 2000;12:581–586.
- McDonald J, Hascall VC. JBiol Chem 2002;277:4575–4579.
- Jiang D et al. Physiol Rev 2011;91:221–264.
- Kessiena L et al. Wound Rep Reg 2014;22:579-593.
- Deed R et al. Int J Cancer, 1997;71:51-56.
- Rajan P et al. Universal Research Journal of Dentistry. 2013;3:113.
- De Boulle K et al. Dermatologic Surgery 2013;39(12):1758-1766
- Longaker T et al. Ann Surg 1991;April:292-296.
- Mast BA et al. Matrix, 1993;13:441-446.
- Asparuhova MB et al. J Periodont Res. 2018;00:1-13.
- Salbach J et al. J Mol Med 2012;90:625-635.Sculean A et al. Med Princ Pract. 2007;16(3):167-80.
- Kitchen JR et al. Biochem J 1995;309:649–656.
- Saranraj P and Naidu MA. IJPBA, 2013;4(5):853–859.
- André, P. J Europ Acad Dermatol Venereol 2004;18:422–425.
- De Boulle K et al. Dermatologic Surgery 2013;39(12):1758-1766.
DOWNLOAD-BEREICH
| Broschüre xHyA |